僇僥僯儞尋媶
僇僪僿儕儞偑宍懺宍惉偵嵟傕廳梫側嵶朎娫愙拝暘巕偱偁傞偙偲傪媈偆恖偼偄側偄偱偟傚偆丅丂偙偺僇僪僿儕儞偺婡擻挷愡傗僔僌僫儖揱払偵娭梌偡傞嵶朎幙懁偺場巕偑夝愅偝傟丄僇僪僿儕儞偺嵶朎幙僪儊僀儞偵捈愙寢崌偡傞抈敀幙偑彮側偔偲傕俀庬椶偁傞偙偲偑抦傜傟偰偄傑偟偨丅丂堦偮偼暘巕検侾侽俀倠俢丄傕偆堦偮偼俋係倠俢偱丄偦傟偧傟兛僇僥僯儞丄兝僇僥僯儞偲屇偽傟偰偄傑偟偨偑丄巹偨偪偑嵶朎娫愙拝憰抲傪扨棧偟偨偙傠偵偼丄偦傟傜偺徻嵶偼晄柧偱偟偨丅丂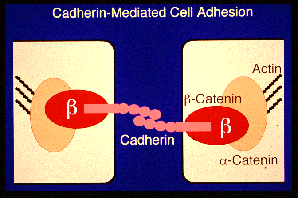 傾僪僿儗儞僗僕儍儞僋僔儑儞偵僇僪僿儕儞偑擹弅偟偰偄傞偺側傜丄偙傟傜偺暘巕傕擹弅偟偰偄傞偱偁傠偆偲偄偆壖掕偺傕偲偵丄変乆偺暘夋偐傜僇僥僯儞丄摿偵丄兛僇僥僯儞傪惛惢偟丄偦偺堚揱巕傪扨棧偡傞偙偲偵弶傔偰惉岟偟丄價儞僉儏儕儞偲偄偆丄傗偼傝愙拝晹埵偺嵶朎幙懁偵擹弅偡傞抈敀幙偵帡偰偄傞偙偲偑暘偐傝傑偟偨丅丂傑偨丄摨偠擭偺廔傢傝偵丄傾儊儕僇偺僌儖乕僾偵傛偭偰丄兝僇僥僯儞偺堚揱巕偑扨棧偝傟丄傾儖儅僕儘堚揱巕偲屇偽傟傞僔儑僂僕儑僂僶僄偺宍懺宍惉堚揱巕偺嶻暔偵帡偰偄傞偙偲偑暘偐傝傑偟偨丅丂偙傟偑丄尰嵼丄偒傢傔偰拲栚偝傟偰偄傞僇僥僯儞偺暘巕惗暔妛偺枊奐偗偱偟偨丅丂尰嵼偱偼丄塃恾偵帵偡傛偆偵丄僇僪僿儕儞偺嵶朎幙僪儊僀儞偵兝僇僥僯儞偑寢崌偟丄偦傟偵兛僇僥僯
傾僪僿儗儞僗僕儍儞僋僔儑儞偵僇僪僿儕儞偑擹弅偟偰偄傞偺側傜丄偙傟傜偺暘巕傕擹弅偟偰偄傞偱偁傠偆偲偄偆壖掕偺傕偲偵丄変乆偺暘夋偐傜僇僥僯儞丄摿偵丄兛僇僥僯儞傪惛惢偟丄偦偺堚揱巕傪扨棧偡傞偙偲偵弶傔偰惉岟偟丄價儞僉儏儕儞偲偄偆丄傗偼傝愙拝晹埵偺嵶朎幙懁偵擹弅偡傞抈敀幙偵帡偰偄傞偙偲偑暘偐傝傑偟偨丅丂傑偨丄摨偠擭偺廔傢傝偵丄傾儊儕僇偺僌儖乕僾偵傛偭偰丄兝僇僥僯儞偺堚揱巕偑扨棧偝傟丄傾儖儅僕儘堚揱巕偲屇偽傟傞僔儑僂僕儑僂僶僄偺宍懺宍惉堚揱巕偺嶻暔偵帡偰偄傞偙偲偑暘偐傝傑偟偨丅丂偙傟偑丄尰嵼丄偒傢傔偰拲栚偝傟偰偄傞僇僥僯儞偺暘巕惗暔妛偺枊奐偗偱偟偨丅丂尰嵼偱偼丄塃恾偵帵偡傛偆偵丄僇僪僿儕儞偺嵶朎幙僪儊僀儞偵兝僇僥僯儞偑寢崌偟丄偦傟偵兛僇僥僯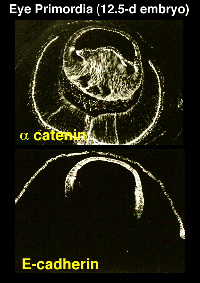 儞偑寢崌偟偰偄傞偙偲丄偝傜偵丄俙俹俠偲屇偽傟傞偑傫梷惂堚揱巕嶻暔偑兝僇僥僯儞偑寢崌偟偰丄兝僇僥僯儞偺暘夝傪惂屼偟偰偄傞偙偲偑柧傜偐偵側偭偰偄傑偡丅丂僇僥僯儞宯偼嵶朎娫愙拝偺儗僊儏儗乕僞乕偲偟偰摥偔偩偗偱側偔丄妀傊堏峴偟偰廳梫側僔僌僫儖揱払暔幙偲偟偰傕摥偄偰偄傞栿偱丄尰嵼偙偺暘栰偼偝傜偵敪揥偟偮偮偁傝傑偡丅
儞偑寢崌偟偰偄傞偙偲丄偝傜偵丄俙俹俠偲屇偽傟傞偑傫梷惂堚揱巕嶻暔偑兝僇僥僯儞偑寢崌偟偰丄兝僇僥僯儞偺暘夝傪惂屼偟偰偄傞偙偲偑柧傜偐偵側偭偰偄傑偡丅丂僇僥僯儞宯偼嵶朎娫愙拝偺儗僊儏儗乕僞乕偲偟偰摥偔偩偗偱側偔丄妀傊堏峴偟偰廳梫側僔僌僫儖揱払暔幙偲偟偰傕摥偄偰偄傞栿偱丄尰嵼偙偺暘栰偼偝傜偵敪揥偟偮偮偁傝傑偡丅
丂嵍恾偵偼丄摉帪丄摼傜傟偨堚揱巕偐傜儕僐儞價僫儞僩偺兛僇僥僯儞抈敀幙傪嶌傝丄偦傟傪峈尨偵偟偰弶傔偰僸僩兛僇僥僯儞傪愼傔傟傞儌僲僋儘乕僫儖峈懱傪摼偰丄偦傟偱愼傔偨嵶朎偺憸傪帵偟傑偡丅偦偺屻丄偙偺尋媶幒偱偼丄兛僇僥僯儞偑偁傞庬偺堓僈儞乮峝偑傫乯偱偦偺敪尰偑柍偔側偭偰偄傞偙偲傪丄崙棫偑傫僙儞僞乕偺峀嫶愢梇攷巑偺尋媶幒偲嫟摨偱尒弌偟丄偑傫壔偲僇僥僯儞偺娭學偵偮偄偰偼偠傔偰柧傜偐偵偟傑偟偨丅丂傑偨丄摉帪丄変乆偺尋媶幒偱島巘傪偟偰偄偨丄塱熀徍椙攷巑偼丄兛僇僥僯儞偲僇僪僿儕儞偺梈崌抈敀幙傪嶌傞偲偄偆曄傢偭偨曽朄偱丄兝僇僥僯儞偺婡擻偵敆傝傑偟偨丅丂塱熀攷巑偼丄嵟嬤丄巹偨偪偺尋媶幒偐傜孎杮戝妛敪惗僙儞僞乕嫵庼偲偟偰撈棫偟丄僇僥僯儞偺尋媶傪懕偗偰偄傑偡丅

 傾僪僿儗儞僗僕儍儞僋僔儑儞偵僇僪僿儕儞偑擹弅偟偰偄傞偺側傜丄偙傟傜偺暘巕傕擹弅偟偰偄傞偱偁傠偆偲偄偆壖掕偺傕偲偵丄変乆偺暘夋偐傜僇僥僯儞丄摿偵丄兛僇僥僯儞傪惛惢偟丄偦偺堚揱巕傪扨棧偡傞偙偲偵弶傔偰惉岟偟丄價儞僉儏儕儞偲偄偆丄傗偼傝愙拝晹埵偺嵶朎幙懁偵擹弅偡傞抈敀幙偵帡偰偄傞偙偲偑暘偐傝傑偟偨丅丂傑偨丄摨偠擭偺廔傢傝偵丄傾儊儕僇偺僌儖乕僾偵傛偭偰丄兝僇僥僯儞偺堚揱巕偑扨棧偝傟丄傾儖儅僕儘堚揱巕偲屇偽傟傞僔儑僂僕儑僂僶僄偺宍懺宍惉堚揱巕偺嶻暔偵帡偰偄傞偙偲偑暘偐傝傑偟偨丅丂偙傟偑丄尰嵼丄偒傢傔偰拲栚偝傟偰偄傞僇僥僯儞偺暘巕惗暔妛偺枊奐偗偱偟偨丅丂尰嵼偱偼丄塃恾偵帵偡傛偆偵丄僇僪僿儕儞偺嵶朎幙僪儊僀儞偵兝僇僥僯儞偑寢崌偟丄偦傟偵兛僇僥僯
傾僪僿儗儞僗僕儍儞僋僔儑儞偵僇僪僿儕儞偑擹弅偟偰偄傞偺側傜丄偙傟傜偺暘巕傕擹弅偟偰偄傞偱偁傠偆偲偄偆壖掕偺傕偲偵丄変乆偺暘夋偐傜僇僥僯儞丄摿偵丄兛僇僥僯儞傪惛惢偟丄偦偺堚揱巕傪扨棧偡傞偙偲偵弶傔偰惉岟偟丄價儞僉儏儕儞偲偄偆丄傗偼傝愙拝晹埵偺嵶朎幙懁偵擹弅偡傞抈敀幙偵帡偰偄傞偙偲偑暘偐傝傑偟偨丅丂傑偨丄摨偠擭偺廔傢傝偵丄傾儊儕僇偺僌儖乕僾偵傛偭偰丄兝僇僥僯儞偺堚揱巕偑扨棧偝傟丄傾儖儅僕儘堚揱巕偲屇偽傟傞僔儑僂僕儑僂僶僄偺宍懺宍惉堚揱巕偺嶻暔偵帡偰偄傞偙偲偑暘偐傝傑偟偨丅丂偙傟偑丄尰嵼丄偒傢傔偰拲栚偝傟偰偄傞僇僥僯儞偺暘巕惗暔妛偺枊奐偗偱偟偨丅丂尰嵼偱偼丄塃恾偵帵偡傛偆偵丄僇僪僿儕儞偺嵶朎幙僪儊僀儞偵兝僇僥僯儞偑寢崌偟丄偦傟偵兛僇僥僯 儞偑寢崌偟偰偄傞偙偲丄偝傜偵丄俙俹俠偲屇偽傟傞偑傫梷惂堚揱巕嶻暔偑兝僇僥僯儞偑寢崌偟偰丄兝僇僥僯儞偺暘夝傪惂屼偟偰偄傞偙偲偑柧傜偐偵側偭偰偄傑偡丅丂僇僥僯儞宯偼嵶朎娫愙拝偺儗僊儏儗乕僞乕偲偟偰摥偔偩偗偱側偔丄妀傊堏峴偟偰廳梫側僔僌僫儖揱払暔幙偲偟偰傕摥偄偰偄傞栿偱丄尰嵼偙偺暘栰偼偝傜偵敪揥偟偮偮偁傝傑偡丅
儞偑寢崌偟偰偄傞偙偲丄偝傜偵丄俙俹俠偲屇偽傟傞偑傫梷惂堚揱巕嶻暔偑兝僇僥僯儞偑寢崌偟偰丄兝僇僥僯儞偺暘夝傪惂屼偟偰偄傞偙偲偑柧傜偐偵側偭偰偄傑偡丅丂僇僥僯儞宯偼嵶朎娫愙拝偺儗僊儏儗乕僞乕偲偟偰摥偔偩偗偱側偔丄妀傊堏峴偟偰廳梫側僔僌僫儖揱払暔幙偲偟偰傕摥偄偰偄傞栿偱丄尰嵼偙偺暘栰偼偝傜偵敪揥偟偮偮偁傝傑偡丅