生命科学の研究は、今、人類が経験したこともないようなエキサイティングな局面を迎えています。反面、皮肉なことに、技術が進みすぎて「手を動かしていれば何か結果が出る」「工場のように分担して研究を進めれば進歩が早くて競争に勝てる」といった状況になっていることも確かで、初めて研究を始めようとする若い人が純粋な夢を持ち続けにくい時代になっていることも確かだと思います。
ひと時代前には、大学院生はよく「研究をエンジョイしているか?」と聞かれたものです。 いま、最先端の研究室では、なかなかこの質問を聞くことができません。 効率を重視して、忙しすぎるのです。 この研究室では、「研究をエンジョイする」ことを基本におきたいと考えています。 少々効率が落ちても、個々の研究者が個々の自覚と責任のもとに研究をエンジョイすることを目指しています。 もちろん、エンジョイするということは、遊ぶことではありません。 うまくいかなくて、能率が悪くて、悩み苦しむことも、エンジョイのうちです。 したがって、この研究室では、基本的には全てのシステムが個々人の自主性を基本としており、一つのテーマを遂行する上で必要な技術は、電子顕微鏡観察から遺伝子工学まで、一人でこなす必要があります。 工場的な組織の中で研究をするより、結果を出すという点でかなり厳しい面がありますが、はるかに研究をエンジョイできると信じてます。
この研究室に集まっている研究者は、大学院生も含め、いろいろなバックグラウンドを持ったヘテロの集団です。 もちろん、医学を勉強したものも1/3くらいいますが、理学部、薬学部、農学部、工学部出身者も全体の2/3を占めます。 それぞれの知識と技術を出し合って、細胞の種々の機能を分子のレベルで語ることに情熱を傾けています。 いわゆる細胞生物学(Cell
Biology)、最近では分子細胞生物学と呼ばれる分野です。
研究の興味の中心は、細胞間接着の分子機構とその制御機構、細胞骨格の構造と機能、さらには、細胞間接着や細胞骨格がかかわるシグナル伝達機構にあります。 特に、多細胞生物において重要な割には注目されていない(トレンディーでない?)細胞種、上皮細胞に焦点を絞っています。
このような研究の結果、何が見えてくるのでしょうか? 基礎学問としての側面と応用学問としての側面を常に意識しています。 基礎的な側面としては、細胞接着や細胞骨格とそのシグナル伝達が上皮細胞の増殖・分化を制御する機構を明らかにしたいと考えていますし、また、上皮細胞シートや内皮細胞シートが多細胞生物の恒常性を保つ上でバリアーとしてどのような役割を果たしているかを分子レベルで明らかにしたい(バリアーの分子生物学)と考えています。 応用面では、悪性腫瘍の90%以上が上皮細胞由来であることから、上皮細胞の理解は細胞のがん化や転移の理解に繋がると考えて研究を進めています。また、バリアーの不全が引き起こす種々の病態に関する解析を進めていきたいと考えています。
よく、我々の分子生物学的研究はユニークだと、純粋な分子生物学の研究者から言われます。言い換えれば、「変わっている」、ということになるのかもしれません。その原因は、解剖学・生化学・生理学と渡り歩いてきた月田自身の経歴によるものかもしれません。生物のある現象に興味をもち、変異体の分離や抗体や薬物による機能阻害といった手法を用いてその現象を担う遺伝子を同定するという、分子生物学の本道とは異なり、私たちの研究のスタートには、常に「形態」があります。「形あるものには機能がある」という前提のもとに、ある「形」、たとえば、ある機能が想定されている細胞内の構造に興味をもち、その構造を構成している蛋白質を分離し、その遺伝子を単離し、そして最後に、その遺伝子を利用して最初に想定した機能に関する分子生物学的解析を行うというやり方です。このような方向の研究は、私たちが研究を始めたころ、すなわちdegenerated primersによるPCRも質量分析によるアミノ酸配列の決定もできなかったころには、多くの技術的な困難を伴いました。しかし、ヒトやマウスの全ゲノムが決定された今、その技術的困難さはほぼすべて解消してしまっているように思います。逆に言うと、私たちが進めてきた研究手法は、いま流行りの「プロテオーム解析」の先駆けだったのかもしれません。
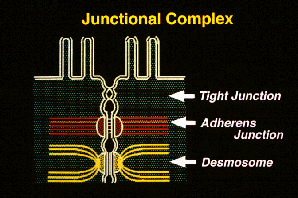 この研究室のすべての研究は、約15年前の「細胞間接着装置の単離法の開発」に始まります。 上述したようなストラテジーに基づいて、上皮細胞間の接着に関与するであろうと思われていた細胞間接着装置を単離しようとしました。 小腸上皮の細胞間接着装置を右図に示しますが、このような単層上皮細胞では、接着装置複合体といって、一般にアピカル側からタイトジャンクション、アドヘレンスジャンクション、デスモソームという異なった3種類の細胞間接着装置が見られます。我々は、最初、これらのうち、カドヘリンと呼ばれる重要な細胞間接着分子が働く場であるアドヘレンスジャンクションに注目し、この構造を単離ようと考えました。 試行錯誤の結果、左図に示すようにラット
(またはマウス)の肝臓からの単離法を開発しました。
この研究室のすべての研究は、約15年前の「細胞間接着装置の単離法の開発」に始まります。 上述したようなストラテジーに基づいて、上皮細胞間の接着に関与するであろうと思われていた細胞間接着装置を単離しようとしました。 小腸上皮の細胞間接着装置を右図に示しますが、このような単層上皮細胞では、接着装置複合体といって、一般にアピカル側からタイトジャンクション、アドヘレンスジャンクション、デスモソームという異なった3種類の細胞間接着装置が見られます。我々は、最初、これらのうち、カドヘリンと呼ばれる重要な細胞間接着分子が働く場であるアドヘレンスジャンクションに注目し、この構造を単離ようと考えました。 試行錯誤の結果、左図に示すようにラット
(またはマウス)の肝臓からの単離法を開発しました。 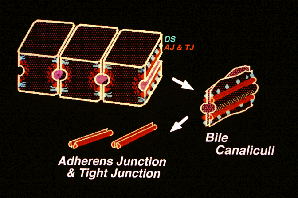 この分画には、予想に反して、タイトジャンクションも濃縮しており、この分画が我々の宝の山となりました。 この分画に濃縮する新しい蛋白質を解析するうちに、いくつかの新らしい研究分野が開けてきました。
この分画には、予想に反して、タイトジャンクションも濃縮しており、この分画が我々の宝の山となりました。 この分画に濃縮する新しい蛋白質を解析するうちに、いくつかの新らしい研究分野が開けてきました。
例えば、この分画から、カドヘリン結合蛋白質であるαカテニンを精製し、そのcDNAを世界で最初にクローニングすることに成功しました。この仕事は、今はきわめて盛んになっているカテニン研究の最初の一歩として広く認められています。このラインの研究は、私たちの研究室から最近独立した永渕昭良教授(熊本大、発生センター)によって、今でも続けられています。